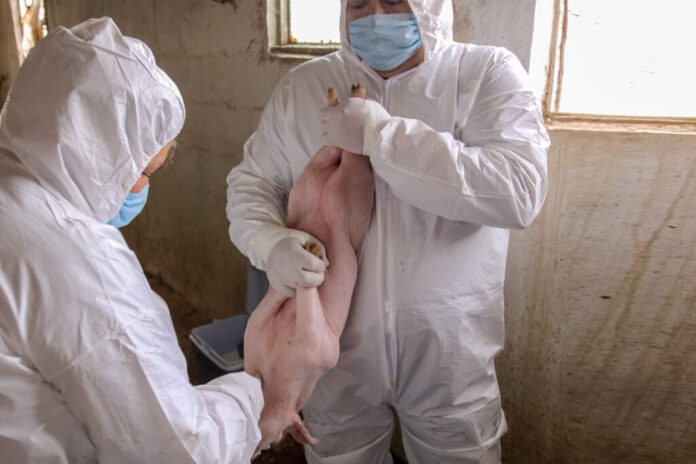
El esquema busca prevenir la falta de eficacia y reacciones adversas en los medicamentos que se suministran a los animales para el tratamiento de plagas y enfermedades, dice la dependencia
Con el objetivo de garantizar la eficacia, calidad y seguridad de los medicamentos utilizados en los animales y, con ello, coadyuvar a la producción de alimentos sanos y seguros, la Secretaría de Agricultura y Desarrollo Rural puso en operación el Sistema de Farmacovigilancia de productos veterinarios.
El Sistema, creado por el Servicio Nacional de Sanidad, Inocuidad y Calidad Agroalimentaria (Senasica), busca identificar, cuantificar, evaluar y prevenir los riesgos asociados a los medicamentos para animales que se comercializan en el territorio nacional y, de esta manera, contribuir a su uso racional.
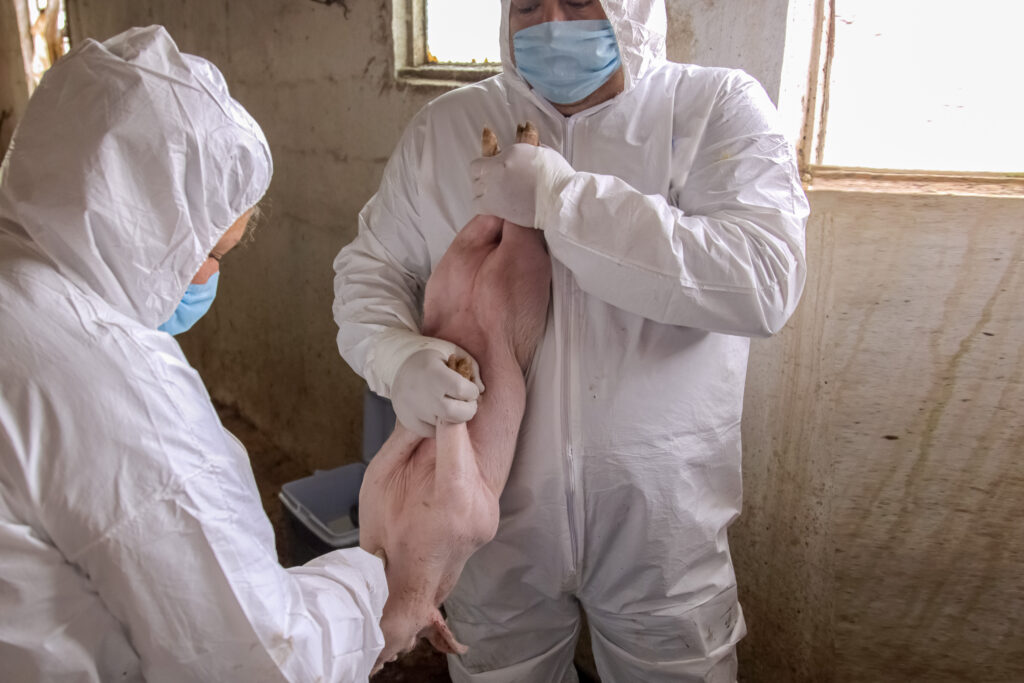
El Sistema de Farmacovigilancia, operado por la Dirección General de Salud Animal, recopila información proveniente de quienes administran productos de uso veterinario, lo que permite identificar reacciones adversas a los medicamentos en cualquier momento de su proceso y así prevenir daños a la salud de los animales
Nuevo marco regulatorio
Con el fin de hacer eficiente y agilizar la atención de eventos adversos de este tipo de medicamentos, en el Sistema intervienen la industria farmacéutica, comercializadoras, distribuidoras, hospitales veterinarios, farmacias, unidades de investigación, médicos veterinarios zootecnistas y todos los profesionales que, de manera directa o indirecta, participan en el manejo de los productos que contribuyen a la procuración de la salud animal.
Como primer paso para la implementación del Sistema de Farmacovigilancia, la Dirección de Servicios y Certificación Pecuaria del Senasica capacitó durante dos días, de manera presencial y virtual, a 84 profesionales de 47 empresas farmacéuticas.
En el evento de presentación del esquema, especialistas del Senasica expusieron la historia de la farmacovigilancia en México durante los últimos 35 años, y explicaron el nuevo marco regulatorio y precisaron los conceptos básicos del tema para que los integrantes de la cadena farmacéutica evalúen la seguridad de sus productos.
Su aplicación será manera gradual
También, se presentó a la industria la “Guía de farmacovigilancia veterinaria para el reporte de eventos adversos (REAS) y la elaboración del reporte periódico de seguridad”, la cual describe las reacciones inesperadas que no están relacionadas con la dosis y no son de origen alérgico.
El documento incluye también el seguimiento a eventos, cuando se sospecha falla en la eficacia esperada de un producto, de acuerdo con lo establecido en la etiqueta; reacciones nocivas en personas después de la exposición a un producto; sospecha de la violación de los límites máximos de residuos (LMR) y problemas ambientales potenciales o la sospecha de transmisión de un agente infeccioso.
El Sistema se aplicará de manera gradual, con el propósito de que se convierta en un instrumento de observancia obligatoria para la industria mexicana dedicada a la producción de químicos, farmacéuticos, biológicos y alimentos para uso veterinario.